Les biostatistiques en 2017 › Les dernières nouveautés réglementaires
Une grande nouveauté en cette rentrée de septembre, avec la publication du très attendu Addendum à ICHE9, la bible du biostatisticien.
Vous le trouverez par exemple ici
L’arrivée de l’addendum à ICHE9 et du concept d’estimand, attendus par les biostatisticiens
Il est sorti le 30 août, mais ce n’est pas une raison pour le laisser passer inaperçu.
Ce n’est pas encore la version finale, puisque des commentaires sont attendus jusqu’en février 2018.
La grande nouveauté est, bien sûr, l’introduction du concept d’estimands, concept qui repose sur une plus grande interaction encore entre cliniciens et biostatisticiens.
L’introduction du concept d’estimands pour les biostatistiques
J’ai eu déjà, pour ma part, la surprise de voir l’EMA demander la rédaction d’un protocole en intégrant des estimands lors d’un scientific advice !…
C’est vrai qu’on en entend parler depuis quelques années maintenant, mais quand même, le mouvement est rapide, il ne faut pas passer à côté, je pense.
Deux événements m’ont permis de mieux comprendre le concept et sa mise en pratique :
- Le congrès international de Biopharmacie et Santé, à Paris, les 14 et 15 septembre,
- Le workshop EFSPI à Bâle, les 4 et 5 Octobre.
Le mot clé à retenir :

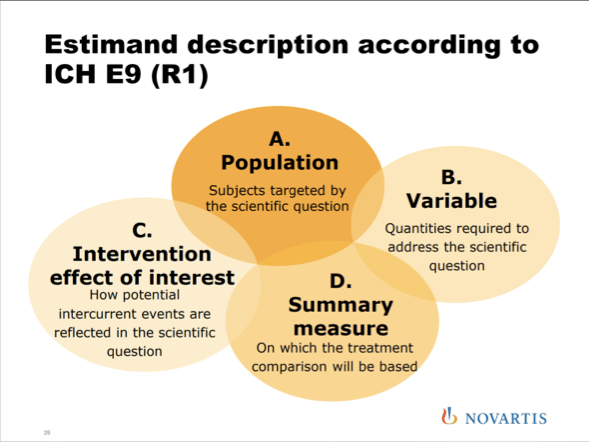
Concevoir un estimand, c’est être capable d’identifier tous les événements intercurrents susceptibles d’intervenir lors d’une étude, et de prédéfinir l’impact que ça aura sur les analyses, en terme de population, d’imputation de données manquantes, d’interprétations…
Les événements intercurrents étant, au choix : la prise d’un traitement de secours, un switch, une mauvaise compliance, un arrêt pour EI, le décès…
Les prochaines étapes pour les biostatistiques
Bref, beaucoup de discussions à prévoir lors de l’écriture du synopsis du protocole, un travail rapproché entre les équipes pour prédéfinir et anticiper le maximum de choses. A gagner, de la clarté dans les objectifs et les interprétations, l’assurance de mesurer ce que l’on veut mesurer, et peut-être au final un moins grand recours à des méthodes de haute technicité dans le domaine des imputations de données manquantes (parfois difficiles à expliciter clairement, il faut l’avouer).
Si on ajoute à ça le draft de guideline FDA sur la multiplicité, on voit qu’on ne s’ennuie pas dans le domaine réglementaire biostat en 2017.
Il est beaucoup plus axé technique que celui de l’EMA, si vous souhaitez trouver des détails sur les méthodes statistiques d’ajustement du risque alpha.
Toutes ces nouvelles notions vont être intégrées dans mes cours et mes offres de conseil de biostatistiques, à Lyon et partout ailleurs.
